|
 |
 |
 |
 |
 |
Modelo Atómico de Thomson A comienzos del siglo XIX se presentaba la siguiente situación:
Por tanto, esas cargas eléctricas debían de estar de alguna forma en el interior de los átomos. Si esto era cierto, la teoría de Dalton era errónea, ya que decía que los átomos eran indivisibles e inalterables. Debido a que no podían verse los átomos, se realizaron experimentos con tubos de descarga o tubos de rayos catódicos y así, de esta manera, se observaron algunos hechos que permitieron descubrir las partículas subatómicas del interior del átomo. Los tubos de rayos catódicos eran tubos de vidrio que contenían un gas a muy baja presión y un polo positivo (ánodo) y otro negativo (cátodo) por donde se hacía pasar una corriente eléctrica con un elevado voltaje.
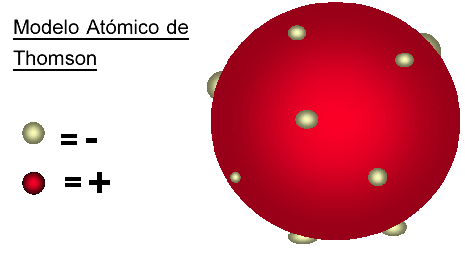
El descubrimiento del electrón Es la primera partícula subatómica que se detecta. Thomson realizó experiencias en tubos de descarga de gases. Observó que se emitían unos rayos desde el polo negativo hacia el positivo, los llamó rayos catódicos. Al estudiar las partículas que formaban estos rayos se observó que eran las mismas siempre, cualquiera que fuese el gas del interior del tubo. Por tanto, en el interior de todos los átomos existían una o más partículas con carga negativa llamadas electrones. Modelo de Thomson Al ser tan pequeña la masa de los electrones, Thomson propuso, en 1904, que la mayor parte de la masa del átomo correspondería a la carga positiva, que ocuparía la mayor parte del volumen atómico. Thomson imaginó el átomo como una especie de esfera positiva continua en la que se encuentran incrustados los electrones, más o menos como las uvas pasas en un pudin.
Este modelo del “pudin de pasas” de Thomson era bastante razonable y fue aceptado durante varios años, ya que explicaba varios fenómenos, por ejemplo los rayos catódicos y los canales: El modelo de Thomson fue bastante valorado ya que era capaz de explicar los siguientes fenómenos: La electrización: el exceso o defecto de electrones que tenga un cuerpo es el responsable de su carga negativa o positiva. La formación de iones: Un ion es un átomo que ha ganado o perdido uno o más electrones. Los electrones se pierden o se ganan con relativa facilidad, de manera que su número dentro del átomo puede variar, mientras que el número de protones es fijo siempre para cada átomo. Si un átomo pierde uno ó más electrones, adquiere carga neta positiva (catión) y si gana uno ó más electrones adquiere carga neta negativa (anión). Para llegar a estas conclusiones Thomson se valió de los siguientes experimentos
|
||||||||||||||